انگل توکسوکانیس و انگل توکسوکارا کتی به ترتیب کرم گرد سگ (آسکاریس) و کرم گرد گربه هستند. این انگلها معمولاً در سگ و گربه یافت می شوند و اغلب توجه زیادی را به عنوان علل احتمالی آلودگی انسانها به خود جلب می کنند. توکسوكاریس لئونينا دیگر کرم گردی است که می تواند سگها و گربه ها را آلوده کند. انسانها میزبانان تصادفی توکسوکارا کنیس و توکسوكارا کتی هستند، اما آلودگی با آنها می تواند منجر به مهاجرت لارو احشایی، مهاجرت لارو چشمی و دیگر سندرم ها به خصوص در کودکان شود. اهمیت نسبی توکسو کارا کنیس و توکسوکارا کتی تا اندازهای مورد بحث است، به دلیل واکنش متقاطع آزمایش های سرمی، به سختی مشخص می گردند. از گذشته تا امروز، گونهی توکسوكارا کنیس علت اصلی آلودگی انسانها است، با این حال، ممکن است اهمیت توکسوكاراکتی به خصوص در بیماری چشمی، دست کم گرفته شود. دراین پست به بررسی انگل توکسوکانیس و انگل توکسوکارا کتی را بررسی میکنیم.
گونه های توکسوکارا و توکسوکانیس
سبب شناسی
آسکاریس ها بزرگ، طویل، غیر بند بند هستند. این انگل ها از نماتودهای روده ای استوانه ای شکل هستند که در روده حیوانات میزبان تولید مثل جنسی دارند. یکی از دوره های تکامل آنها در خارج از بدن و روی خاک است. توکسوكارا کنیس رایج ترین کرم گرد سگ سانان است. توکسوكارا کتی رایج ترین کرم گرد گربهها است. مشخص نیست که توكسوکارا کتی، سگها و توکسوكاراکنیس، گربه ها را آلوده می کند یا خیر. توکسوکاریس لئونینا را در سگها و گربه ها می توان یافت. توکسوكارا مالاینسیس گونه ی دیگر شناخته شده در گربه است. توکسوكارا میستاکس مترادف توکسوكارا کتی است. بیماری زایی این گونه ها با انسان مشخص نیست.
چرخه ی زندگی
کرمهای گرد بالغ در روده کوچک میزبانان زندگی می کنند. تخم های فاقد جنین در مدفوع گذاشته می شوند و در محیط به لاروهای مرحله “سه عفونی” تبدیل می شوند. معمولاً توکسوكارا کنیس و توکسوکارا کتی ۲ تا ۴ هفته زمان برای عفونی شدن نیاز دارند، مدت این زمان تحت تأثیر شرایط محیطی تغییر می کند. لاروهای عفونی زا می توانند در دمای طی ۹ تا ۱۵ روز ایجاد شوند اما در به ۳۵ روز زمان نیاز دارند. لاروهای توکسواکاریس لئونینا ممکن است طی زمان کوتاه، طی یک هفته عفونی زا شوند. میزبانهای مستعد از راه بلعیدن تخمهای عفونی زا یا از طریق خوردن حیواناتی که در بافت های آنها لاروها وجود دارند (میزبانهای حد واسط) آلوده می شوند. کرمهای خاکی و البته دیگر بی مهرگان می توانند لاروها را در روده های خود حفظ کرده و در هنگام خورده شدن، می توانند آلودگی را منتقل کنند.
زمانی که میزبانان نهایی تخم های عفونی را می بلعند، توکوکارا کنیس و توکسوکارا کتی از طریق دیواره روده به کبد و سرانجام به ریه ها مهاجرت می کنند. بعد از رسیدن به ریه ها، لاروها به همراه سرفه بالا آمده و بلعیده می شوند و در روده کوچک به کرمهای بالغ تبدیل می شوند و چرخه زندگی آنها کامل می گردد. بعضی لاروها در بافت ها در مرحله خفته باقی می مانند. بعد از خورده شدن میزبان حد واسط آلوده، لاروها معمولاً مهاجرت نمی کنند؛ ولی در روده کوچک به کرمهای بالغ تبدیل می شوند. لاروهای توکسوکاریس لئونینا صرف نظر از منبع آلودگی، در میزبانان نهایی مهاجرت خارج رودهای ندارند.
دوره خفتگی توکسوکار کنیس ۲ تا ۵ هفته است، در حالی که این دورره در توکسوکارا کتی تقریباً ۸ هفته و در توکساسکاریس لئونینا ۸ الی ۱۱ هفته طول می کشد.
بعد از خوردن تخم های آلوده توسط دیگر میزبانان حدواسط، لاروها به پوشش روده نفوذ کرده و در سرتاسر بدن مهاجرت می کنند. لاروها در میزابانان حدواسط، برخلاف میزبانان نهایی، قادر به رشد و کامل کردن چرخه زندگی خود نیستند. مهاجرت ممکن است برای سال ها و معمولاً به شکل متناوب ادامه می یابد و بیماری بالینی در اثر مهاجرت و واکنش آماسی مرتبط با آن ایجاد می گردد.
امکان انتقال توکسوكارا کنیس به توله سگها از طریق جفت وجود دارد. این حالت در صورت آلودگی حاد در سگهای ماده ایجاد می شود ولی به شکل اولیه با واکنش تأخیری لاروها در بافت ها (در اواخر آبستنی) و متعاقب آن آلودگی رحم مرتبط است. شواهدی مبنی بر آلودگی با توکسوکارا کتی یا توکسوکاریس لئونینا از طریق جفت وجود ندارد.
شیر دادن منجر به انتقال آلودگی به توله سگ ها و بچه گربه ها می گردد. آلودگی از طریق شیر، تنها در صورت آلودگی مزمن گربه ها، حضور تعدادی لارو سماتیک و آلودگی در اواخر آبستنی گربه ی ماده ایجاد میشود. سگ های ماده با خوردن لاروهای موجود در مدفوع توله سگ ها مجدداً آلوده می شوند.
توزیع جغرافیایی / همه گیر شناسی
سگ ها و گربه ها
گونه های توکسوكارا معمولاً گسترش جهانی دارند، به خصوص در بچه گربه ها، توله سگهای جوان، حیوانات شکاری و محل نگهداری آنها، توکسوکاراکنیس از طریق رحمی انتقال می یابد. توکسوکارا کتی و توکسواراکنیس می توانند در زمان شیردهی منتقل شوند و همزمان با تبدیل تخمها به لارو، تعداد انگلها در توله سگها و بچه گربه ها افزایش می یابد. اغلب فرض می شود که تقریباً همه توله سگها آلوده به توکسوكاراکنیس متولد می شوند؛ هر چند این مطلب بر اساس داده های قدیمی بوده و صحت درستی آن نامشخص است. میزان شیوع با توجه به عوامل مختلفی همچون سن، موقعیت جغرافیایی (به عنوان مثال نگهداری در منزل، پناهگاه یا شکاری) و انگل تراپی در سگها و گربه ها متفاوت است. در مطالعات انجام گرفته درباره ی حیوانات ولگرد یا در پناهگاه ها شیوع توکسوکارا در مدفوع را در محدوده 3/5 تا ۸۲ درصد (در سگها) و 8/0 تا 54 درصد (در گربه ها) گزارش کرده اند. توله سگها بیشتر از سگهای بالغ شکاری آلوده می شوند. شیوع این انگل در گربه ها و سگ های بالغی که در منزل نگهداری می شوند پایین تر و معمولاً 4> درصد (در کشورهای توسعه یافته) است. همچنین توکسوكارا کنیس و توکسوکارا کتی در بچه گربه ها نسبت به بالغین رایج تر (بیش از ۳۳ درصد) است. همچنین میزان شیوع در گربه های منازل حیاطدار نسبت به گربه های آپارتمانی بیشتر است. به نظر می رسد گربه های نگهداری شده در منازل حیاط دار اجازه دسترسی بیشتری به محیط خارج خانه نسبت به آنهایی که در آپارتمان زندگی می کنند را دارند. توکسوکاریس لئونينا شیوع کمتری دارد (۳۲> درصد) و این میزان به منطقه ی جغرافیایی بستگی دارد.
راه های آلودگی انسان
بیماری توکسوکاریاز انسان را در تمام امکان حضور سگها و گربه ها، می توان مشاهده کرد، اما شیوع آن مناطق مختلف بسیار متغیر است. میزبان نهایی این انگل ها، سگها و گربه ها (به همراه سگ سانان و گربه سانان وحشی) هستند، به همین سبب در آلودگی انسانها نقش مشخصی دارند. به هر حال تعیین نقش حیوانات خانگی در مقابل حیوانات شکاری و این که آیا آنها منبع مستقیم آلودگی (در مقابل منبع غیر مستقیم آلودگی از محیط آلوده خارج از خانه) هستند یا خیر، مشکل است.
آلودگی انسانها معمولاً بعد از خوردن تخم های عفونی را از خاکهای آلوده، خوردن لاروهای موجود در بافتهای میزبانان حدواسط آلوده (به عنوان مثال، كبدهای نپخته گاو، مرغ، اردک و خوک) و یا خوردن میوهها و سبزیجاتی که به خوبی شسته یا پخته نشده اند، ایجاد می شود.
انتقال از راه تماس مستقیم با سگها و گربه ها به دلیل زمان بر بودن عفونی زا شدن تخمها کم است، با این وجود نگرانی ها تخمهای عفونی زای روی پوشش مویی سگها افزایش یافته است. در مطالعات مختلف تخمهای توکسوکارا درباره ی پوشش مویی سگها را گزارش کرده اند، از جمله آلودگی ۶۷ درصد سگها (بیشتر توله سگها) نژاد پوند در ایرلند. در مطالعه دیگری در ترکیه حضور تخم های توکسوكارا روی سگها (اساساً جوانها) را ۲۲ درصد گزارش کردند ، در این مطالعه، تنها ۸ درصد تخمها دارای جنین بودند و قابلیت عفونی زایی داشتند. تعداد تخم ها در این مطالعات به مقدار کم، ۸ تا ۱۲ تخم جنین دار در هر گرم مو، گزارش شد. در مطالعه ای دیگر در ۱۲ درصد از سگها تخم های توکسوكارا شناسایی شد، اما هیچکدام قابلیت حیات نداشتند، در حالی که در مطالعه دیگری شیوع تخم های توکسوکارا کنیس را در ۲۵ درصد سگها گزارش کرد؛ که 2/4 درصد از آنها دارای جنین و ۲۴ درصد در حال تشکیل جنین بود. پوشش مویی یک حیوان آلوده منحصراً منبع آلودگی نیست، ممکن است تخمها از حیوانات دیگر روی پوشش مویی قرار گرفته باشند. تماس با تخم های موجود در محيط خارج از خانه ممکن است منبع آلودگی باشد. توجه به این مهم برای پیشگیری از آلودگی در انسان ضروری است، در حالی که برای مهار توکسوکارا در حیوانات خانگی لازم نیست از خطر برخورد با پوشش مویی حیواناتی که اجازه خروج از خانه را دارند، اجتناب نمود. میزان خطر آلودگی انسان از پوشش مویی مشخص نیست، خصوصاً به دلیل حضور اندک تخم عفونی زا. نویسنده ای برآورد کرده که از ۳۰۰ تخم در یک گرم مو، ۴درصد دارای جنین هستند، همچنین تعیین کرده که یک فرد باید بیش از ۴ گرم مو بخورد تا ۵۰ تخم عفونیزا وارد بدنش بشود. به همین سبب این سطح فراتر از دریافت تصادفی است. از آن جایی که گربه ها بر طبق عادت دائما خود را تمییز می کنند، نگرانی در خصوص پوشش مویی آنها کم است، اما در گربه های ضعیف یا چاق که به خوبی خود را تمیز نمی کنند، گربه هایی با پوشش مویی بلند و اغشته به مدفوع در ناحیه پرینه، یا گربه های در تماس نزدیک با محل های به شدت آلوده، نگرانی بیشتری وجود دارد. تاکنون شواهدی در خصوص انتقال آلودگی از طریق جفت در گربه ها وجود ندارد.
آلودگی محیط خارج از خانه در بسیاری از مناطق رایج است. میزان آلودگی از نمونه های پارکها، زمین های بازی و حیاطهای خانوادگی کمتر از ۱ تا ۵۵ درصد گزارش شده است. توانایی زنده ماندن تخم های عفونی را برای مدت طولانی در شرایط آب و هوایی متفاوت، باعث افزایش تراکم تخم های عفونی زا می شود.
شیوع سرمی در انسان ها
شیوع عیار پادتن خیلی بیشتر از شیوع خود بیماری است. میزان شیوع سرمی به منطقه جغرافیایی و فاکتورهای خطر مواجهه با انگل، بستگی دارد. این میزان 6/1 تا ۸۵ درصد گزارش شده است، بالاترین میزان شیوع مربوط به مناطق روستایی، مناطق ضعیف و یا مناطق گرمسیری است. افزایش شیوع سرمی، به سن وابسته است، موارد مثبت در نرها بیشتر از ماده ها است. البته تفاوت هایی در افرادی که در خارج از منزل بازی یا کار میکنند وجود دارد.
در مطالعات فراوانی گزارش شده است که نگهداری از سگ یک فاکتور افزاینده سطح پادتن بدن می باشد، با وجود این که منبع آلودگی احتمالاً محیط است. نگهدای از سگها تماس منظم با سگها یا حضور سگها در خانه از فاکتورهای خطر شیوع سرمی در کودکان و همچنین عواملی برای OLM هستند. اینکه داشتن حیوان خانگی خطری آشکاری است یا خیر همچنان مشخص نیست. در خانواده های صاحب سگ، به دلیل آلودگی محیط خانه و افزایش برخورد با امکان آلودهی خارج از خانه (به عنوان مثال، پارکهای عمومی) احتمال شیوع بیشتر است. در مطالعهای ارتباط معنی دار بین شیوع سرمی و نگهداری حیوان خانگی اما بدون حضور آنها در منزل گزارش شده است.
خطر مواجه سگ های پرورشی، به دلیل شیوع زیاد در توله سگهای جوان و احتمالاً آلودگی قابل توجه محیط زیست، ممکن است بیشتر باشد. این مطلب در مطالعه ای درباره ی سرم سگها اثبات شد، در این مطالعه شیوع ۱۶ درصدی سگ پرورشی بریتیش در مقابل 6/2 درصدی گروه کنترل گزارش شد. همچنین نقش محیط آلوده پرورش سگ توسط مطالعات دیگری تأیید شده است. میزان شیوع سرمی در افرادی که تماس مکرر با سگها و گربه ها دارند؛ مانند کارمندان دامپزشکی، کارگران پناهگاههای سگها و پرورش دهندگان گربه در مقایسه با انسان های دیگر بیشتر است. پژوهشگران فاکتورهای دیگر افزاینده سطح سرمی پادتن را موارد زیر می دانند: غذای آلوده، زندگی در مناطق روستایی، رفتن مکرر به زمین بازی، تأخیر رشد در کودکان، کاهش نمرات ضریب هوشی در کودکان، وضعیت های اقتصادی-اجتماعی پایین، بازی مکرر در گودال شنی و تماس مکرر با خاک. تمامی این موارد با افزایش احتمالی خوردن مستقیم یا غیر مستقیم خاک و بهداشت ضعیف در ارتباط هستند. جای تعجب نیست که شستن دست ها قبل از خوردن در کودکان به عنوان یک فاکتور محافظت کننده گزارش شده است.
بیماری در انسانها
هرچند گزارشاتی مربوط به شیوع سرمی این انگل در انسان وجود دارد، اما اطلاعات اندکی در مورد بیماری بالینی وجود دارد. احتمالاً ارتباط معنی داری بین مناطقی با شیوع بالا و بروز بیماری وجود دارد. احتمالاً فاکتورهای خطر افزاینده سطوح پادتن بدن، فاکتورهای خطر برای آلودگی نیز هستند؛ با این حال به مطالعه چشمی محدود شده است. از همین روی با توجه به داده های مربوط به شیوع سرمی مناطق یا جوامع پر خطر می توان خطر ابتلا به بیماری در مناطق دیگر را پیش بینی کرد. به نظر می رسد که وقوع آلودگی در بسیاری از مناطق اندک است. با توجه به تعداد کم داده ها و شدت بالقوه بیماری، باید بیماری توکسوکاریاز به عنوان عامل تهدید کننده ی بیماری مشترک به طور منطقی مورد توجه قرار گیرد.
VLM و OLM دو بیماری مهم مرتبط با آسکاریس های سگ و گربه در انسان هستند، هر چند سندرمهای دیگری نیز می تواند ایجاد شود. بیماری های مشترک انسان و حیوانات خانگی اغلب با توکسوكارا کنیس در ارتباط اند، اما توکسوكارا کتی نیز می تواند منجر به ایجاد بیماری شود. بیماری VLM اغلب در کودکان کمتر از ۴ تا ۶ سال ایجاد می شود، به خصوص در کودکانی با سابقه ی گنده خواری یا آنهایی که در شرایط غیر بهداشتی زندگی می کنند. توکسوکای من خورده شدن می تواند در تمام بافت های بدن مهاجرت کند، گاهی وارد یک مرحله خفتگی شده و سپس مهاجرت بیشتری انجام می دهد. توانایی به خواب رفتن و فعال شدن دوباره، به این معنی است که بیماری به خوبی بعد از آلودگی رخ میدهد و مدت زمان دوره کمون مشخص نیست. آلودگی اغلب بدون علامت است، افزایش پادتن های سرمی که تنها تغییر قابل تشخیص است، البته آلودگی و مرگ ناگهانی می تواند ایجاد شود. بروز بیماری به فاکتورهای مختلفی بستگی دارد، از جمله تعداد لاروها و بافت هایی که به آنها مهاجرت کرده اند.
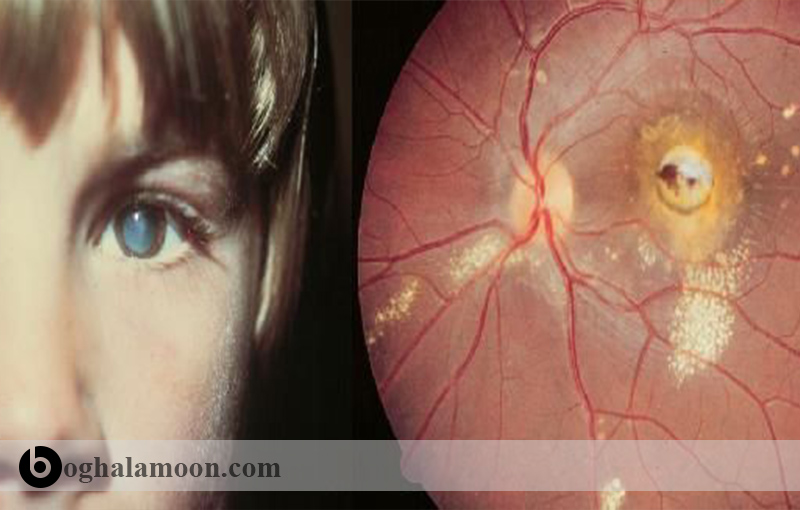
مهاجرت لاروهای توکسوکارا به داخل چشم موجب بیماری OLM می گردد. معمولاً فقط یک لارو درگیر است و آلودگی تقریباً همیشه به صورت یک طرفه است. بیماری OLM احتمالاً از مهاجرت انتخابی لارو به داخل چشم ایجاد می شود و در آنجا یک توده آماسی ائوزینوفیلیک ایجاد می کند. بیماری VLM در کودکان رایج تر است، اما انگل به افرادی که چند سالی مسن تر هستند بیشتر از افرادی دچار VLM تمایل دارد. به نظر می رسد بیماری OLM بسیار نادر باشد. یک مطالعه بزرگ آمریکایی وقوع بیماری را در دانش آموزان ابتدایی 6/6 تا 7/9 درصد (در ۱۰۰,۰۰۰ نفر) برآورد کرده است، در حالی که در مطالعه آمریکایی دیگر، وقوع بیماری را یک مورد در هر ۱۰۰۰ نفر برآورد کرده است و در یک مطالعه درباره ی کودکان در ایرلند با بررسی بیش از ۲۰۰۰ کودک، هیچ موردی از بیماری OLM شناسایی نشد. وقوع همزمان VLM و OLM بسیار نادر است اما می تواند ایجاد شود.
دیگر تظاهرات آلودگی به مهاجرت توکسوکارا به بافت ها و واکنش سیستم ایمنی افراد درگیر بستگی دارد. به نظر می رسد آلودگی با توکسوکارا، یکی از علت های وسیع آلرژی و بیماری های آماسی است. نتایج مطالعات متعدد انجام شده جهت شناسایی نقش احتمال توکسوکارا در آسم کودکان متناقضی بوده است. همچنین این انگل را به عنوان یکی از علل صرع دانسته اند، هر چند همه ی مطالعات این ارتباط را تایید نمی کنند، آلودگی با این انگل با اختلالات دیگر مانند کهیر مزمن، خارش مزمن، اگزما و رنیت آلرژی و ائوزینوفیلی ناشناخته نیز، در ارتباط است.
حیوانات
نشانه های بالینی
سگها
بیماری در سگها معمولاً تحت بالینی است، بیماری های بالینی اساساً در توله سگها دیده می شوند. توله سگها به همراه بیماری توکسوكارا کنیس معمولاً علائمی مانند عدم رشد، عدم توانایی در وزن گیری، پوشش مویی ضعیف و شکمی با ظاهر قابلمه ای شکل دارند. در موارد نادر، بیماری شدید یا مرگ ناگهانی می تواند ایجاد گردد. بعضی توله سگها که میزان قابل توجهی کرم دارند، ممکن است تعداد زیادی کرم را با استفراغ از بدن خود خارج کنند.
در نتیجه مهاجرت لاروها از طریق کبد می تواند زخمهایی را ایجاد کند، اما به ندرت نشانه های قابل تشخیص ایجاد می کند. در مقابل، مهاجرت تعداد زیادی لارو از طریق ریه ها می تواند منجر به بیماری تنفسی (که با خونریزی و آماس همراه است) گردد. این حالت در توله سگهای جوانی که تعداد زیادی توکسوكارا کنیس را از طریق رحم دریافت کرده اند، رایج است.
بیماری بالینی در بالغین غیر معمول است و می تواند از یک التهاب رودهای خفیف تا انسداد روده (در مواردی که تعداد کرمی زیاد باشد) متغییر باشد. استفراغ به واسطه تحریک معده توسط مهاجرت لاروها از مخاط، میتواند ایجاد شود. لارو مهاجر گزارش شده، اما به نظر می رسد خیلی نادر باشد. بیماری OLM در برخی سگ ها از حمله سگ های کارگر گله می تواند مشکل ساز شود، هر چند اطالاعات روشنی وجود ندارد.
بیماری بالینی به واسطه آلودگی با توکساسکاریس لئونينا نادر است و به خوبی شرح داده نشده است.
گربه ها
از آنجا که آلودگی رحمی در گربه ایجاد نمی شود، بچه گربه ها در زمان آلودگی سن بالاتری در مقایسه با توله سگها دارند و بیماری بالینی تا قبل از آن ایجاد نمی شود. بیماری بالینی در بچه گربه ها می تواند مشابه آن چه که در بالا برای توله سگها شرح داده شد، باشد. با این تفاوت که بچه گربه ها در زمان آلودگی بزرگتر بوده بنابراین ممکن است علائم بالینی آشکار و شدید در آنها کمتر ایجاد گردد. علائم خفیف، به خصوص شکم با ظاهر قابلمه ای شکل ممکن است تنها علائم بالینی ایجاد شده باشد. دفع تخمها مهم تر از بیماری بالینی است و مدرک آشکاری وجود دارد که بچه گربه ها تا ۳ هفته می توانند تخم انگل را دفع کنند.
مشابه سگها، بیماری بالینی در گربه های بالغ غیر معمول است. ممکن است علائم غیر اختصاصی مانند پوشش مویی ضعیف، اسهال و شکمی با ظاهر قابلمه ای شکل دیده شود.
تشخیص
علائم بالینی غیراختصاصی است اما در بچه گربه ها و توله سگها مطرح شده اند، به خصوص آنهایی که فاقد یا سابقه ی بسیار ناچیزی از آلودگی انگلی را داشته اند. شناسایی کرم ها در مواردی که استفراغ وجود دارد، جنبه تشخیصی دارد.
تشخیص بیش تر بر اساس شناسایی تخم ها در مدفوع با استفاده از روش شناورسازی سانتریفیوژی است. معمولاً تعداد زیادی تخم به شکل منظم دیده می شوند، اما تشخیص همیشه ساده نیست. تفریق تخم های توکسوکارا از تخم های بایلیساسکاریس بروسيونيس بسیار سخت است؛ با این حال، بايليساسكاريس بروسيونيس در سگها و گربه ها بسیار نادر است. دوره نهفتگی ۲ تا ۴ هفته است.
مدیریت
فنبندازول، میلبمایسین اکسیم، نیتروسکانات، موکسی دکتين، فبانتل و پیرانتل پاموات داروهای مؤثر در سگها و گربه ها هستند. پیپرازین را می توان استفاده کرد ولی اثر کمتری نسبت به دیگر گزینه ها دارد. برای درمان توکسوكارا کتی در گربه ها، امودپساید مؤثر است. اغلب داروهایی که ماهانه برای پیشگیری از کرم قلب استفاده می شوند، بر آسکاریس ها هم مؤثر هستند. مشخص شده که پیشگیری دارویی، ابتدایی ترین اقدامات پیشگیرانه است. تاکنون مقاومت در برابر ضد انگل ها در مورد گونه های توکسوكارا شناسایی نشده است.
انسان ها
نشانه های بالینی
VLM
اغلب آلودگی ها بدون علامت هستند. افرادی با بیماری بالینی، می توانند علائمی از خفیف تا مرگ برق آسا داشته باشند. بیماری خفیف ممکن است با علائم غیراختصاصی مانند سرفه، تب، خس خس و بزرگ شدن کبد مشخص گردد که در نتیجه مهاجرت از طریق کبد و ریه ها هستند. همچنین ممکن است بی اشتهایی، سر درد، کاهش وزن، خستگی و شکم درد وجود داشته باشد. از ریه درگیر نیز می توان رادیوگراف تهیه کرد، هرچند بیماری شدید تنفسی نادر است. در میزان اندکی از موارد، ممکن است بزرگ شدن طحال وجود داشته باشد. آماس عضله قلب از دیگر تظاهرات نادر بیماری است. وقوع همزمان با بیماری OLM مرسوم نیست ولی ممکن است ایجاد شود.
مشاهدهی بیماری عصبی معمول نیست (برخلاف لارو مهاجر بایلیساسکاریس بروسیونیس) اما حملات صرعی ممکن است ایجاد شود. در بیمارانی که لارو مهاجر عصبی دارند؛ سر درد، تب و دیگر نشانه های عصبی یا سیستمیک غیراختصاصی نیز ممکن است وجود داشته باشد.
OLM
در این شکل از بیماری، اندوفتالمیت و آماس شبکیه رایج است. علائم بالینی ممکن است شامل از دست دادن قدرت دید، لوکوکوریا، لوچی، پارس پلانتیس و گرانولوم یا جداشدگی شبکیه باشد. در بعضی از بیماران قدرت بینایی کم نمی شود ولی در برخی دیگر به شدت کاهش می یابد. کور شدن معمول نیست ول می تواند اتفاق بیفتد. درگیری هر دو چشم نادر است. علائم سیستمیک مانند بزرگ شدن کبد و تب معمولاً وجود ندارند.
نشانه های بالینی دیگر
بیماری های دیگری با علائم متفاوت و شدید، به همراه اسکاریس های مشترک بین انسان و دام ممکن است وجود داشته باشند. ائوزینوفیلی غیراختصاصی به علت واکنش بدن به لاروهای مهاجر ممکن است وجود داشته باشد. مهاجرت لارو معمول است و منجر به ائوزینوفیلی می گردد. در تمام موارد ائوزینوفیلی بدون علت، مهاجرت لارو باید بررسی شود. یک ارتباط بین پادتن های ضد توکسوکارا و کهیر مزمن بدن مشخص شده است.
تشخیص
VLM
ائوزینوفیلی یک علامت کلاسیک است و بیماری VLM باید در هر بیماری (به ویژه هر کودک) با ائوزینوفیلی غیر قابل توجیه مورد توجه قرار گیرد. افزایش تعداد گلبولهای سفید خون و هایپرگاماگلوبولینمی نیز ممکن است وجود داشته باشد. برخورد احتمالی با عوامل پرخطر خصوصاً گنده خواری باید مد نظر قرار گیرند.
یکی دیگر از روش های تشخیصی، یافتن لاروها در بیوپسی بافتهای آلوده (به عنوان مثال کبد) است. علت حضور نادر لاروها در بافت، پاسخ آماسی ایجاد شده نسبت به پوشش خارجی انگل است که مکرراً در طی مهاجرت جدا می شوند، از همین روی ممکن است لاروها در محل فعالیت آماسی حضور نداشته باشند. حضور پادتن های ضد توکسوکارا تائیدی بر این بیماری است، اما به دلیل اینکه ممکن است افراد بدون علامت نیز سرم مثبت باشند، قطعی نیست. ارزش اخباری داده های سرم شناسی مثبت به شیوع عیار سرمی پایه در جمعیت بستگی دارد.
OLM
بیماری OLM در کودکانی نابینا و لوچ، باید مورد توجه قرار گیرد. تشخیص عمدتاً بر اساس علائم بالینی در زمان معاینه چشم صورت می گیرد. ممکن است گرانولوم قطب خلفی چشم که شبیه رتینوبلاستوما است مشاهده گردد؛ اولتراسونوگرافی برای تفریق این دو مفید است. پادتن سرم به علت منفی بودن در برخی افراد مبتلا به OLM و مثبت بودن در برخی از افراد سالم، چندان کمک کننده نیست.
شناسایی سطوح بالای پادتن در مایع زلالیه در مقابل سرم خون، ممکن است از نظر تشخیصی مفید باشد. ائوزینوفیلی محیطی نادر است.
سایر روشهای تشخیصی
تشخیص سایر نشانه های بالینی به دلیل طبیعت غیر آشکار بیماری ممکن است مشکل باشد. مثبت بودن سرم به همراه حضور علائم بالینی را می توان به آلودگی با توکسوکارا نسبت داد، اما پیچیدگی خاصی در عیار سرمی جمعیت های سالم وجود دارد.
مدیریت
VLM
اغلب افراد بیماری خفیفی دارند و بدون درمان بهبود می یابند. در افرادی با بیماری شدید مانند بیماری عصبی یا بیماری شدید تنفسی درمان صورت می گیرد. آلبندازول داروی انتخابی است. کورتیکواستروئیدها در بیمارانی با درگیری سیستم عصبی مرکزی یا قلبی ممکن مورد استفاده قرار گیرد.
OLM
رهیافت استانداردی برای بیماری OLM وجود ندارد و درمان آن اغلب موفقیت آمیز نبوده، چراکه معمولاً بین شروع آلودگی و تشخیص فاصله ی زمانی زیادی وجود دارد. یکی از ضدانگل های مورد استفاده آلبندازول است، اما استفاده از داروهای ضدانگل به علت ایجاد آماس شدید و تهدید بینایی (به واسطه مرگ لاروها) ممنوع شده است. تزریق کورتیکواستروئید ممکن است آماس چشم را کاهش دهد. ویترکتومی اغلب مورد نیاز است.
روش های دیگر مدیریت
انجام اقدامات درمانی به شدت بیماری و سندرم بستگی دارد. بسیاری از تظاهرات بیماری خود محدود شونده هستند و بدون درمان بر طرف می شوند. درمان با استفاده از ضد التهاب ها و ضد انگل ها می تواند مد نظر قرار گیرد.
پیشگیری
کرم زدایی سگها و گربه ها
تمام توله سگ و بچه گربه الوده باید بررسی شوند و کرم زدایی مناسب در این حیوانات ضروری است. تمامی توله سگها باید با پیرانتل پاموات، فنبندازول یا میلبمایسین اکسیم در ۲، ۴، ۶ و ۸ هفتگی، سپس ماهانه تا ۶ ماهگی کرم زدایی شوند. کرم زدایی بچه گربه ها باید در ۳ هفتگی آغاز گردد. فرزندان حیوانات شیرده باید در زمان مشابه درمان شوند. اگر سگهای ماده قبل از آبستنی آلودگی اندکی با توکسوکارا کنیس داشته اند، باید در زمان آبستنی با فنبندازول به صورت روزانه یا آیورمکتین دو تا چهار بار درمان شوند.
درمان های متقاضی برای حیوانات بیش از ۶ ماهه توصیه شده است و شامل کرم زدایی ماهانه، یک یا دو بار در سال، یا حداقل چهار بار در سال با فاصله حداقل سه ماه است. درمان بر اساس بررسی مدفوع در محل زندگی در مناطق کم خطر (بدون درمان پیشگیرانه و منظم) نیز پیشنهاد شده است. فاکتورهایی که هنگام پیشگیری از کرم گرد باید مورد توجه قرار گیرند شامل: شیوع کرم گرد در منطقه، وضعیت پرورش حیوانات، مدیریت حیوانات خانگی، تعداد حیوانات خانگی نگهداری شده در منزل و این که آیا افراد با خطر بالا (به عنوان مثال، کودک مبتلا به گنده خواری) در خانه حضور دارند یا خیر، است.
بررسی مدفوع سگها و گربه ها
مدفوع باید به صورت دوره ای بررسی شود تا نیاز به کرم زدایی و ارزیابی اثر بخشی برنامه های پیشگیرانه مشخص گردد.
جهت بررسی مدفوع انجام آزمایش دو تا چهار بار در سال اول و بعد از آن یک یا دو بار در سال توصیه شده است. روش های سانتریفیوژی به دلیل بالاتر بودن حساسیتشان نسبت به روش های شناورسازی گرانشی باید مورد استفاده قرار گیرند.
کاهش مواجهه سگها و گربه های خانگی
محدودیت قرارگیری حیوانات خانگی نگهداری شده در منزل (اما محدود نشده) در فضای باز خارج از منزل (به خصوص در فضاهای باز و مهار نشده با احتمال خوردن مدفوع آلوده یا میزبانان حدواسط مرده) به کاهش خطر مواجهه کمک می کند.
کاهش درگیری انسانها
جلوگیری از تماس با مدفوع ها در محیط، یک اقدام مهاری منطقی است ولی ممکن است مشکل باشد. یکی از اقدامات مهاری مهم، حذف سريع مدفوع های گذاشته شده در محیط است چرا که اولاً تخم ها برای عفونی شدن به زمان نیاز دارند و ثانیاً ممکن است شواهدی از آلودگی مدفوعی در محیطی که تخم های آلوده حضور دارند مشاهده نشود. اما، برداشتن منظم مدفوع ها از جعبه های نگهداری حیوانات خانگی از تشکیل تخمهای آلوده جلوگیری خواهد کرد.
ضدعفونی محیط به دلیل مشکلاتی که در حذف بیماری زاها از محیط های غنی از مواد آلی وجود دارد و همچنین مقاومت محیطی انگل ها، اقدامی مشکل یا غیر ممکن است. استفاده از ضد عفونی کننده ها در فضای بیرون عملی نیست. دما نقش مهمی در گسترش و مقاومت تخم ها در محیط ایفا می کند. در دمای پایین تر از ، رشد لاروها متوقف می شود و در درجه دمای یا پایین تر، لاروها از بین میروند. تمیز کردن لانه هایی که مادران برای توله سگها و بچه گربه ها خود آماده کرده اند، امکان آلودگی تصادفی با مدفوع موجود در محیط را کم می نماید. به دلیل مقاومت تخم های توکسوكاراها به اغلب ضد عفونی کنندهها، حذف فیزیکی تخم ها از روی سطوح اهمیت دارد.
سرانجام، آلودگی انسانها مستلزم بلعیدن تخم های دارای لارو است، بنابراین باید توجه زیادی به بهداشت دست ها، به خصوص بعد از تماس با محیطهای با خطر زیاد (به عنوان مثال، محیط زیست توله سگ/ بچه گربه) یا حیوانات داشت. کودکان مستقیماً نظارت شوند تا از خوردن خاک، شن، مدفوع یا سایر اشیائی که قابلیت آلودگی دارند، اجتناب گردد. این امر به ویژه برای کودکان با اشخاص دیگری که تمایل به خوردن خاک یا گنده خواری دارند صادق است. همچنین بهداشت دست ها بعد از کار یا بازی کردن در بیرون از خانه اهمیت دارد. هر زمانی که امکان دارد باید جعبه های شنی را پوشاند تا گربه ها در آن ها مدفوع نکنند. در بعضی از شهرها به دلیل خطر لاروهای مهاجر، جعبه های شنی پارکهای شهرداری را برداشته اند.
هیچ توصیه خاصی برای پیشگیری دارویی بعد از مواجهه (مانند زمانی که کودک در حال خوردن خاک آلوده است) وجود ندارد.
آموزش نگهداری حیوانات خانگی یا غیر خانگی (جهت افزایش آگاهی از اقدام مهاری مناسب برای حیوانات خانگی)، حمل مناسب مدفوع و اجتناب از خوردن سهوی خاک آلوده، اهمیت دارد. مدرک اهمیت انجام اقدامات پیشگیری کننده از آلودگی در افراد عادی جامعه کم است. در یک مطالعه بریتانیایی، دانش نگه دارندگان حیوانات خانگی نسبت به نگه دارندگان حیوانات غير خانگی، در برابر توکسوکاریاز مشترک بین انسان و دام بیشتر نبود و اطلاعات آنها در مورد آلودگی انسان ها یا حیوانات با توکسوکا را پایین بود.








































































































































































































نظرات کاربران
2:27:55 AM